РАНДОМИЗИРОВАННЫЕ КОНТРОЛИРУЕМЫЕ
КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ
Что такое РКИ? Рандомизированныеконтролируемые клинические исследования (РКИ) проводятся с серединыпрошлого века. Их гуманистическая направленность стала ответом научногосообщества на проведение экспериментов на людях во время Второй мировойвойны в фашистских концлагерях. РКИ являются фундаментом доказательноймедицины, так как на их основе происходит принятие научно-обоснованныхрешений и проводится мета-анализ. Поэтому целесообразно более подробноостановиться на особенностях их планирования и проведения. РКИпредполагают использование тонких и чувствительных операционных истатистических методов во время проспективного исследования, в которомсопоставляемые группы получают различные виды анализируемыхвмешательств, лица контрольной группы — стандартное по современнымпредставлениям лечение.
Отличительной особенностьюсовременных РКИ является неукоснительное следование этическим нормам.Перед началом любого РКИ его протокол должен быть одобрен национальнымили региональным этическим комитетом (часто и тем, и другим). Вдальнейшем этический комитет в обязательном порядке информируется осерьезных побочных эффектах, возникших в ходе РКИ и всех изменениях впротоколе. До включения в исследование его потенциальный участник долженна добровольной основе подписать информированное согласие, где вдоступной форме должна быть изложена цель исследования, возможныеосложнения или неудобства, преимущества, связанные с участием больного висследовании, и альтернативные методы лечения. Пациент должен бытьпроинформирован о том, что решение о его участии или неучастии в данномклиническом исследовании на любом этапе выполнения никак не отразится надальнейшей тактике его ведения, и он в любой момент может прекратитьсвое участие в РКИ. Только после получения информированного согласияпациент может принимать участие в исследовании. Если РКИ предполагаетпроведение суб-исследований,требующих дополнительного обследования, то на них тоже необходимополучить информированное согласие пациента. В ряде случаев, например припроведении РКИ у детей, информированное согласие подписывают родителиили опекуны.
ЦЕЛИ И ЗАДАЧИ ИССЛЕДОВАНИЯ
Дляоценки новых методов лечения и диагностики могут применяться дваосновных вида исследования — контролируемые и неконтролируемые.Неконтролируемое клиническое испытание (без сравнения с ужеприменяющимся способом терапии или плацебо) новых методов лечениядопустимо только в исключительных случаях, когда новый метод позволяетспасти жизнь или радикально улучшить прогноз у пациентов, страдающихнеизлечимым заболеванием (в настоящее время большинство такихисследований связано с ВИЧ-инфекцией). Необходимо подчеркнуть, что даже вэтом случае предполагаемая польза нового метода должна бытьубедительной и сопоставимой, например, с эффектом инсулина при сахарномдиабете I типа.
Особняком стоят неконтролируемыеклинические испытания при изучении новых лекарственных препаратов наэтапе фазы I и II их клинического исследования, когда на здоровыхдобровольцах и ограниченном числе пациентов определяютсяфармакокинетические и фармакодинамические характеристики нового методалечения.
Актуальность проведения контролируемыхклинических исследований в настоящее время существенно возросла, так какони необходимы не только для доказательной медицины, но и привыполнении рутинной научной работы, в том числе и диссертационныхисследований клинической направленности.
ПланированиеРКИ начинается с формулирования цели и задач исследования, которыеотличаются новизной и практической значимостью. Цель исследования должнаотличаться как научной новизной, так и практической значимостью.Например, именно таким исследованием было SYST-EUR, результаты которого взначительной степени реабилитировали антагонисты кальция в леченииартериальной гипертензии, когда на них обрушилась волна критики порезультатам не совсем корректного мета-анализа.
Поэтому,как правило, крупные многоцентровые РКИ планируют известные в своейобласти специалисты. Каждое новое РКИ оригинально по дизайну и популяциипациентов, участвующих в нем (определяется критериями включения иисключения), поэтому уже существующие протоколы не могут быть полностьювоспроизведены вновь, хотя и могут служить некой базой для адаптации. Вкачестве примера решения сходной задачи можно привести два сильноразличающихся как по дизайну, так по итоговым результатам протоколаисследований ALLHAT и ASCOT. Точная формулировка основной цели имеетрешающее значение. Так, можно в качестве примера привести исследованиеELITE I, в котором сравнивалась эффективность ингибитора АПФ каптоприла иантагониста рецепторов ангиотензина II лозартана у пациентов схронической сердечной недостаточностью. Достоверных различий между этимидвумя режимами терапии не выявлено, но цель исследования была «доказатьпреимущества лозартана», и она не была достигнута. Однако новый класспрепаратов, оказавшийся не хуже эталонных ингибиторов АПФ, стал важнымсобытием для кардиологов. Если бы целью исследования было доказательстворавнозначной эффективности лозартана и каптоприла при хроническойсердечной недостаточности, никакой последующей полемики попросту невозникло.
Задачи, решаемые в РКИ, не должны бытьмногочисленными, поскольку это может привести к ложноположительнымрезультатам и затруднить интерпретацию полученных данных для практики.
КОНЕЧНЫЕ ТОЧКИ
Существуют«жесткие» и «мягкие» (суррогатные) конечные точки, оцениваемые в РКИ. Кжестким конечным точкам относят, например, общую и сердечно-сосудистуюсмертность, инсульт, инфаркт миокарда. Примерами суррогатных конечныхточек являются гипертрофия левого желудочка, фракция выброса, уровеньлипидов, глюкозы крови т.д. R.J. Temple определяет суррогатные конечныеточки как «…косвенный критерий оценки в клиническом испытании -лабораторный показатель или симптом, который заменяет клиническизначимый исход, прямо характеризующий самочувствие больного, егофункциональное состояние и выживание. Изменения косвенного
критерияоценки, вызываемые лечением, должны отражать изменения клиническизначимого критерия (исхода)». Необходимость использования суррогатныхконечных точек обусловлена тем, что для получения статистическидостоверного влияния вмешательства на жесткие точки необходимообследовать большое число пациентов и наблюдать их на протяжениидлительного времени. Суррогатные конечные точки (типичные для каждойнозологии) позволяют существенно уменьшить длительность исследования иколичество больных, участвующих в нем. Однако обязательно нужно помнить:выбранные суррогатные точки должны иметь доказанное влияние на прогнозисследуемого заболевания. Безусловно, выбранным конечным точкамнеобходимо иметь не только научное, но и клиническое значение.Предпочтение отдается объективным (например, развитие инсульта,подтвержденное компьютерной томографией), стандартизованным критериям(индекс массы миокарда левого желудочка по данным эхокардиографии) идискретным показателям эффективности (показатели типа да/нет, жив/умер,госпитализация/отсутствие госпитализации, улучшение/ухудшение), покоторым рассчитывается абсолютный и относительный эффект вмешательства иих легко интерпретировать практическому врачу.
Вмногих РКИ выделяют основные конечные точки, по которым оцениваетсяэффективность вмешательства, и второстепенные конечные точки,учитывающие другие аспекты этого вмешательства (например, побочныеэффекты, качество жизни, когнитивные нарушения, лабораторные показатели ит.д.). Хотя в ряде случаев последние сами могут становиться основнойконечной точкой (например, когнитивные изменения в исследовании SCOPE,холестерин — в исследованиях по атеросклерозу, уровень креатинина — висследованиях по почечной недостаточности, артериальной гипертензии исахарному диабету).
Впоследнее время в РКИ стали широко использоваться так называемыекомбинированные конечные точки, объединяющие сразу несколькопоказателей. Например, в исследовании PREAMI конечной точкой являлсяпоказатель смерть + госпитализация с сердечной недостаточностью +сердечное ремоделирование. Как видно, здесь использованы как жесткие,так и суррогатные конечные точки.
Существеннооблегчить задачу по выбору оптимальных конечных точек при планированииисследований может использование существующих баз данных о клиническихисходах (табл. 7.1).
Таблица 7.1. Источники информации рекомендуемых для оценки клинических показателях при проведении исследований

Ещеодной особенностью современных РКИ является проведение суб-исследований(суб-протоколов) в рамках основного РКИ, которые используютдополнительные методы обследования и позволяют ответить надополнительные вопросы, остававшиеся за рамками основного РКИ.
Длительность исследования (интервал времени от момента рандомизации больного и осуществления вмешательства до момента
оценкиконечного исхода заболевания) определяется целью и задачамиисследования, зависит от характера патологии, особенностей естественноготечения заболевания, риска развития исследуемых осложнений и времени,необходимого вмешательству для оказания потенциального влияния навыбранные конечные точки.
ВЫБОР БОЛЬНЫХ
Вторымпо значимости разделом РКИ (после формулирования цели и задачисследования) является определение критериев включения и исключения изисследования. Критерии включения предопределяются целью исследования,более широкие из них облегчают набор пациентов и позволяютэкстраполировать полученные результаты на большую популяцию больных.Однако в этом случае существует опасность формирования разнородныхисследуемых групп больных как по исходным клинико-демографическимпоказателям, так и по эффективности тестируемого вмешательства. Обычно вРКИ включают пациентов со средней тяжестью заболевания, хотя упациентов с исходно более высоким риском осложнений можно в болеекороткие сроки оценить эффект вмешательства на жесткие конечные точки.Группа пациентов с низким риском и легким течением заболевания требуетдлительного наблюдения и потенциально опасна в получении статистическидостоверного эффекта вмешательства, тогда как на самом деле оно можетоказаться эффективным.
Критерииисключения должны минимизировать возможность ошибок при проведенииисследования (например, исключение из исследования больных стерминальной стадией заболевания, сниженной функцией печени и почек).Если данный контингент пациентов не является предметом РКИ, в негообычно не включают несовершеннолетних, женщин в период беременности илактации или не использующих контрацепцию, онкологических и психическихбольных. Важной задачей критериев исключения является обеспечениеодинакового лечения и ведение пациентов в исследуемой и контрольнойгруппах, а также исключение применения в них во время исследованияпрепаратов, сходных с испытуемым.
В целом чем крупнееРКИ и чем быстрее его планируют закончить, шире должны быть критериивключения и тем меньше критериев исключения.
РАЗМЕР ИССЛЕДОВАНИЯ
Никакихнормативов, кроме получения необходимой статистической достоверностипри определении числа пациентов, участвующих в исследовании, несуществует. Небольшое количество пациентов не позволяет добитьсяоднородности сравниваемых групп и статистически достоверного эффектавмешательства. Размер РКИ зависит от ожидаемого клинически значимогоэффекта вмешательства.
Типичным исходным показателем,необходимым для расчета размера РКИ, является ожидаемый исходзаболевания при стандартном общепринятом лечении на момент планированияисследования. Кроме этого, весьма полезными оказываются данныезакончившихся РКИ по аналогичной тематике.
Принятосчитать, что снижение относительного риска исхода заболевания на 20%является клинически значимым. При этом степень достоверности полученияложноположительного обычно устанавливается на уровне 0,05 («а» или «Iтип ошибки»). В свою очередь степень достоверности ложноотрицательногорезультата обычно устанавливается на уровне 0,1 («b» или «II типошибки»).
РазмерРКИ, в котором в качестве критериев эффективности вмешательстваиспользуются дискретные показатели исхода заболевания, всегда больше,чем размер такого же РКИ, но в котором критерием эффективностивмешательства являются продолженные показатели исхода заболевания(средние величины показателя или функционального исхода).
Достаточностьгрупп наблюдения зависит от степени предполагаемых различий в эффектевмешательства в опытной и контрольной группах, видом статистическогопоказателя эффекта вмешательства (частоты, средние величины).Естественно, чем больше ожидаемое различие в эффекте между ними, темменьше окажется необходимое число наблюдений.
Приодинаковой степени точности необходимое число наблюдений будетзначительно меньше, когда для оценки эффекта вмешательства используютсясредние величины, а не частотные показатели.
Припроведении исследования очень важно получить достоверную информацию обэффективности вмешательства в возможно более сжатые сроки. Для этогоиспользуют многоцентровые РКИ. В них происходит кооперирование (частомеждународное) и стандартизация исследовательских центров по единойпрограмме и методам наблюдения, что позволяет получить сопоставимыеданные разных учреждений.
РАНДОМИЗАЦИЯ
Надежностьданных РКИ прямо зависит от сопоставимости сравниваемых групп.Категорически нельзя сравнивать группы, в одну из которых были включеныпациенты с анализируемым вмешательством, а в другую — отказавшиеся отучастия в РКИ и получавшие «традиционную» терапию. Также нельзясопоставлять результаты нового метода лечения в разных клиниках, еслиони не проводили его оценку по одному общему протоколу (различий втехнической оснащенности, квалификации кадров и принятых стандартахлечения). Аналогичные недостатки имеет и метод «исторического контроля».
Одноиз обязательных условий надежности исследования — сопоставимостьсравниваемых групп. Очень часто в публикуемых исследованиях нарушаетсяэтот важнейший принцип. Например, группы несопоставимы, если в одну изних включаются больные, леченные новым методом, а в другую -отказавшиеся от него. Согласие больного подвергнуться лечению новымметодом зависит от типа нервной деятельности, степени выраженностизаболевания, общего состояния, возраста и прочих факторов, которые могутиметь прогностическое значение. Иногда сопоставляются результаты новогометода лечения, проводимого в одной клинике, с эффективностьюстандартного способа лечения, используемого в других лечебныхучреждениях. В этом случае неоднородность групп еще больше увеличиваетсяза счет различий в технической оснащенности и квалификации кадров,использования разных вспомогательных лечебных методов и прочего.Примерно такими же недостатками характеризуется метод так называемого«исторического контроля», когда сопоставляются результаты лечения довнедрения нового метода с эффективностью современного лечения, т.е.сравнивают специально подобранную для применения нового метода лечениягруппу больных с неподобранной группой «прошлого». К рандомизации такжене относятся методы, при которых больных распределяют в опытную иконтрольную группы в порядке поступления, по начальным буквам имен ифамилий, по нечетным и четным дням включения в исследование, дате днярождения. При таком отборе врач может предвзято включить пациента схорошим, по его мнению, эффектом от вмешательства в «правильную» группу инаоборот.
Рандомизация является ключевым моментом при проведении РКИ. Она должна обеспечить случайное распределение больных, независящее от желания врача или каких-либо других факторов, исопоставимость сравниваемых групп по клинико-демографическимхарактеристикам пациентов, тяжести основного исследуемого заболевания,сопутствующей патологии и проводимой терапии.
Принебольшом числе пациентов в группах даже правильно проведеннаярандомизация не может обеспечить их однородность. В этом случаеиспользуется предварительная стратификация (stratum — слой,пласт), при которой распределение вариантов вмешательства происходит вболее однородных группах больных, изначально сформированных по одномуили нескольким важным признакам. Различия пациентов по этим ключевымпризнакам должны быть минимальными. Такой подход практически гарантируетполучение надежных результатов и отсутствие систематической ошибки.Отсутствие систематической ошибки в РКИ называют обоснованностью(validity).
Наиболее частой причиной несопоставимостисравниваемых групп после рандомизации может быть включение в анализ невсех участвовавших в исследовании пациентов.
Существуетбольшое количество методов рандомизации: метод непрозрачныхзапечатанных и последовательно пронумерованных конвертов, компьютерныйметод (процедура рандомизации на основе метода генерации случайных чиселпроводится специалистом, непосредственно не участвующим в лечении),метод пронумерованных идентичных контейнеров, подготовленныхфармацевтической фирмой (код и истинное содержание контейнеров неизвестны ни пациентам, ни врачам, участвующим в исследовании),централизованная рандомизация по телефону (IVRS) специалистомфармацевтической фирмы. Наиболее объективным считается последний из них,а наименее объективным — метод конвертов.
Прирандомизации необходимо соблюсти одно важное условие — непредсказуемыйхарактер распределения больных на группы (нельзя предугадать, в группувмешательства или контроля попадет пациент). Ни пациент, ниисследователь не должны знать, в какие группы попадают пациенты. Этодостигается при использовании «слепого», «двойного слепого» и даже«тройного слепого» отбора. Если о назначаемом вмешательстве известнотолько врачу, такая организация РКИ называется «простым слепымиспытанием» (single-blind trial). Если все лица исследовательскогоцентра, общающиесяи работающие с пациентами, не знают, кто из них какое лечение получает,то это «двойное слепое испытание» (double-blind trial). Подобнаяорганизация РКИ абсолютно необходима в тех случаях, когда велика рольсопутствующего лечения, например при антибиотико- и химиотерапии.
Частопроцесс «ослепления» достаточно сложен, например традиционная терапияпредполагает применение таблетированных форм, а новое вмешательствоиспользует инъекции. В этом случае в первой группе лечение придетсядополнить введением физиологического раствора, а во втором — приемомплацебо per os. Нелишне отметить, что вид, органолептические свойства и кратность назначения сравниваемых препаратов должны быть одинаковыми.
В настоящее время существует несколько причин, по которым в научных исследованиях рандомизация не используется:
• незнание врачами-исследователями основ доказательной медицины;
• слепое следование традиционной практике и боязнь получить результаты, отличные от общепринятых и мнения авторитетов;
• боязнь применить у пациента менее эффективный метод вмешательства, ноименно ради выявления его реальной эффективности проводится РКИ;
• существующее негативное общественное мнение, отождествляющее РКИ с испытаниями на людях.
Втоже время в последние годы термин «рандомизация» стал использоватьсяавторами публикаций как «магическое заклинание», гарантирующее авторамотсутствие критики и повышающее их научный рейтинг самооценки. Истиннаярандомизация подменяется ее декларированием, проявляетсянесопоставимостью сравниваемых групп и «информационным шумом» от выводовпо некачественно сделанным исследованиям. Так, K.F. Schultz et al.считают, что только 9-15% статей в медицинских журналах имели истиннуюрандомизацию.
ДИЗАЙН ИССЛЕДОВАНИЙ
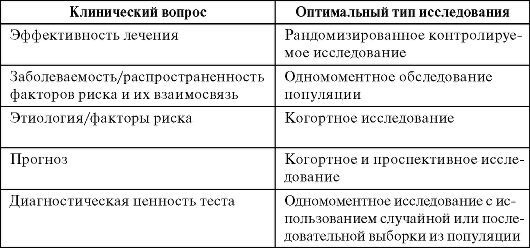
Сегоднядля решения конкретного клинического вопроса идентифицированыоптимальные типы (табл. 7.2) и дизайны (рис. 7.1) исследований. Каждыйиз видов исследований имеет свои достоинства и недостатки (табл. 7.4).
Таблица 7.2. Клинические вопросы и оптимальные типы исследований для их решения
Важнопонять, что структура исследования, в существенной мерепредопределяемая поставленным клиническим вопросом, прямо влияет настепень доказательности полученных данных (табл. 7.3).

Рис. 7.1. Наиболее часто используемые дизайны проведения клинических исследований
Таблица 7.3. Уровень доказательности исследований в зависимости от их структуры при оценке эффективности вмешательства
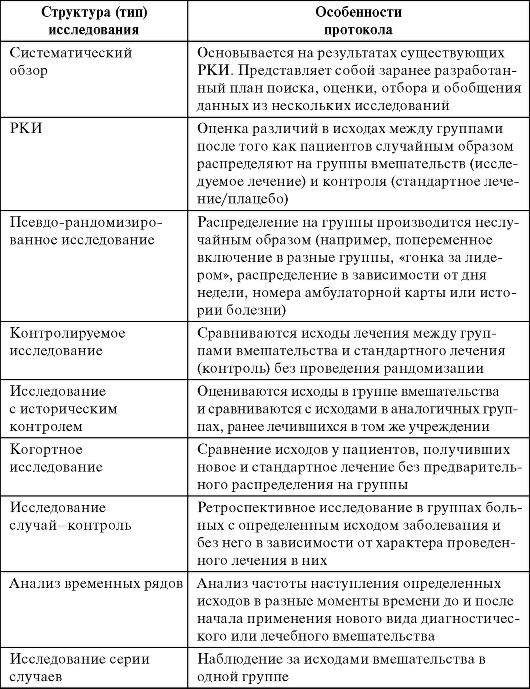

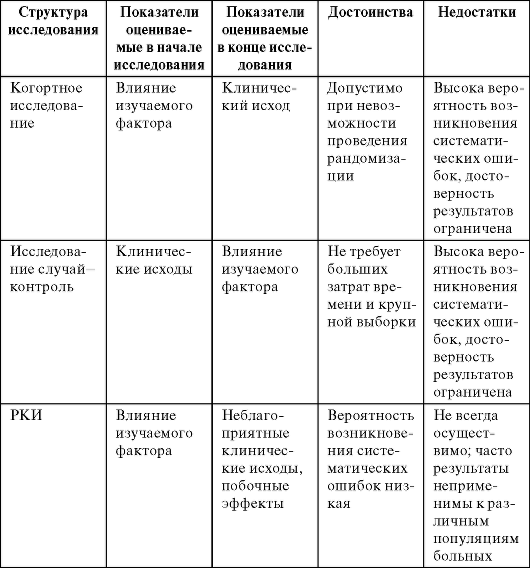
Таблица 7.4. Достоинства и недостатки исследований с различной структурой
АНАЛИЗ И ИНТЕРПРЕТАЦИЯ РЕЗУЛЬТАТОВ
Главной задачей статистического анализа РКИ является установление разницы и степени ее достоверности по исходам (конечным
точкам)между группой с анализируемым вмешательством и контрольной группой. Внастоящее время существует много пакетов статических программ дляанализа полученных результатов (BMDP, SOLO, Statistica и другие). Дляполучения объективной информации об эффективности вмешательства в анализнеобходимо включать всех первоначально рандомизированных больных(intention-to-treat analysis), а не только тех, которым лечениепроведено в строгом соответствии с протоколом исследования (on protocolanalysis). Это один из основных способов минимизировать возможныеошибки, когда при intention-to-treat analysis исходят из допущения, чтовсе пациенты получили лечение, предписанное при рандомизации.
Выбываниепациентов из исследования по разным причинам (отказ от дальнейшегоучастия, побочные эффекты и плохая переносимость лечения, нарушенияпротокола пациентами или исследователями) не должно превышать 15% отисходного числа рандомизированных больных. Если процент выше, результатыисследования некорректны. Такой подход существенно снижает вероятностьполучения ложноположительного результата, когда на самом деле онотсутствует. Считается: если более 80% из включенных больных наблюдалисьдо конца исследования, его результаты могут быть достаточно надежными.
Длястатистического анализа большого массива дискретных конечных точеквычисляют c-квадрат. При малой выборке (число пациентов менее 30 вкаждой из групп вмешательства) используют методы непараметрическойстатистики (тесты Фишера или Йетса).
Результатыисследования представляются с использованием следующих показателей:число больных, которых необходимо пролечить для того, чтобыпредотвратить один нежелательный исход заболевания,абсолютного/относительного риска нежелательного исхода и их снижения суказанием статистической достоверности.
ПУБЛИКАЦИЯ РЕЗУЛЬТАТОВ
Частостатью с итогами РКИ предваряет опубликование его наиболее значимыхрезультатов и выводов в материалах крупных международных конференций исъездов. Структура статьи имеет обычный характер. Обязательнымтребованием является максимально широкое представление дизайна истатистических аспектов РКИ. Особый интерес может представлятьобсуждение результатов, так как они
могут дать дополнительную информацию о спорных моментах при его проведении.
Внастоящее время для проведения РКИ разработаны этические иметодологические стандарты. Необходимо помнить о том, чтоплацебо-контролируемые исследования оправданы, когда не существуетальтернативного способа лечения, эффективность которого не вызываетсомнений.
Сегодня врачам, исследователям иорганизаторам исследований необходимо непрерывно повышать не толькопрофессионализм, но и уровень знаний в области доказательной медицины,правоведения и GCP. При этом само проведение РКИ — не только наука, но иособый (и достаточно прибыльный) медицинский бизнес, что предъявляетеще более высокие этические требования ко всем его участникам.
Литература
1. Pocock S.J. Clinical trials. A practical approach. — John Wiley & Sons
Ltd., 1983.
2. Guyatt G.H. etal. Users’ guides to the medical literature. II. How to use an articleabout therapy or prevention. A. Are the results of the study valid //JAMA. — 1993. — Vol. 270. — Р. 2598-2601.
3. Guyatt G.H. etal. Users’ guides to the medical literature. II. How to use an articleabout therapy or prevention. B. What were the results and will they helpme in caring for my patients // JAMA. — 1994. — Vol. 271. — P. 59-63.
4. Begg C. et al. Improving the quality of reporting of randomized controlled trials. The CONSORT statement // JAMA. — 1996. — Vol. 276 —
P. 637-639.