Статиновая афера
Сразу оговорюсь, что я не ставлю своей целью, какое-либо якобы разоблачение фармацевтического заговора в контексте применения статиновых препаратов. Нет, мне просто хотелось рассказать об альтернативном взгляде в научном мире на проблематику обоснованности использования статинов для профилактики и лечения сердечно-сосудистых заболеваний и атеросклероза, и снижения уровней "плохого" холестерина.
«Я пришел к осознанию того, что холестерин не является ужасным врагом человека, в чем нас пытались убедить, вместо этого я понял, что холестерин — одно из самых важных веществ в нашем организме, вещество, без которого жизнь, какой мы ее знаем, просто прекратила бы свое существование. То, что миллиарды долларов были потрачены на полномасштабную войну с веществом, которое жизненно необходимо для нашего здоровья, без сомнения, является величайшей научной карикатурой нашей эры», Дуэйн Грэйвлайн, доктор медицинских наук, и астронавт, один из шести ученых, отобранных НАСА для программы «Аполлон».
Тезисное резюме [1,2] прежде чем мы начнем:
1. Положительные эффекты статиновых препаратов были в значительной мере преувеличены, а кроме того, эти эффекты не имеют ничего общего со способностью данных препаратов снижать уровень холестерина.
2. Статиновые препараты приводят к истощению запасов коэнзима Q10 — одного из наиболее важных для сердца пищевых веществ. Недостаток Q10 может вызывать мышечные боли, слабость и утомление.
3. Холестерин необходим мозгу для оптимального функционирования. Холестерин помогает стимулировать мыслительную деятельность и память.
4. По данным сразу нескольких исследований, статиновые препараты снижают количество половых гормонов. Сексуальная дисфункция — это распространенный (но малоизвестный) побочный эффект статиновых препаратов.
5. Статиновые препараты блокируют деятельность серотониновых рецепторов в мозгу.
6. Возникают тревожные сигналы о том, что статиновые препараты могут повышать риск возникновения рака и диабета.
7. Всестороннее исследование, проведенное исследователем из Медицинской школы при Калифорнийском университете в Сан- Диего, показало, что большинство врачей просто отказываются принимать жалобы своих пациентов о побочных эффектах статинов и не сообщают о них в MedWatch — учрежденную Администрацией по контролю за продуктами питания и лекарствами США систему сбора информации о нежелательных эффектах медицинских продуктов или лекарств (эффектов, которые носят собирательное название «нежелательные явления»). Иначе говоря, информация о побочных эффектах чрезвычайно плохо освещена.
8. Статины нельзя выписывать пожилым людям и подавляющему большинству женщин, и они ни в коем случае не должны выписываться детям.
9. Исследования показывают, что (за редким исключением) некоторые положительные результаты от приема статиновых препаратов получают только мужчины среднего возраста, у которых точно установлена ишемическая болезнь сердца. Точнее для данной категории людей, польза от приема статинов может превышать риски, хотя на самом деле эта "польза", оценивается очень незначительными показателями измеряемыми в абсолютных процентных значениях, плюс все присущие негативные риски от использования статинов, никуда не деваются.
На сегодняшний день статины являются препаратами выбора для лечения больных сердечно-сосудистыми заболеваниями [3]. Считается, что способность улучшать прогноз как у лиц с сердечно-сосудистыми заболеваниями, так и с высоким риском их развития подтверждена результатами крупномасштабных рандомизированных исследований, что по идее должно выделять данную группу лекарств среди других гиполипидемических препаратов [4,5].
Правда существуют достаточно серьезные проблемы с качеством публикуемых крупных исследований, доказывающие пользу статинов. В большинстве своем, они финансирутся самими фармацевтическими компаниями, прямая заинтересованность которых в повышении продаж статинов очевидна. Нет, безусловно нельзя говорить о том, что по этой причине проводимые исследования недействительны, но не упомянуть о данном факте все равно стоит.
Статины — одни из самых популярных лекарственных средств на сегодняшний день, и их популярность среди врачей, продолжает неуклонно расти, и опять же в немалой степени благодаря активному лоббированию статинов фармкомпаниями, в том числе среди медицинского профессионального сообщества.
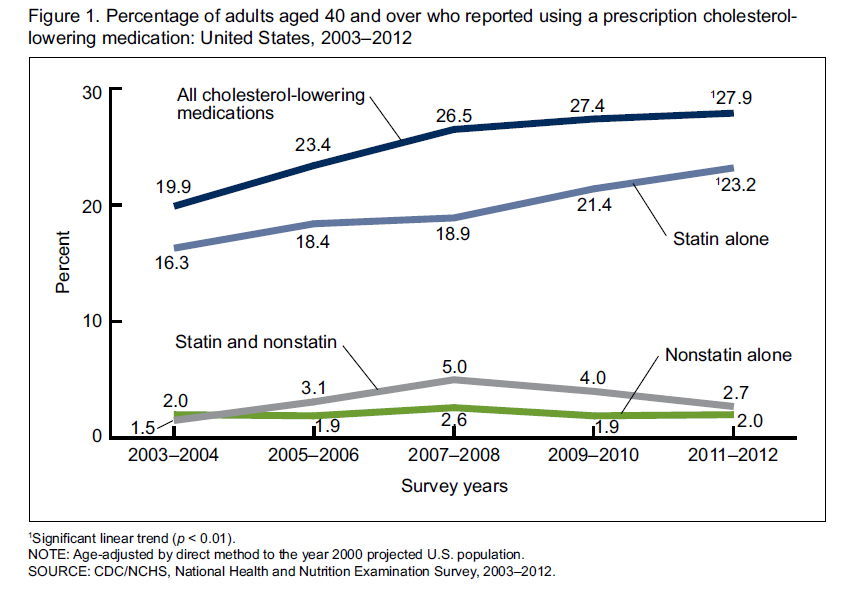
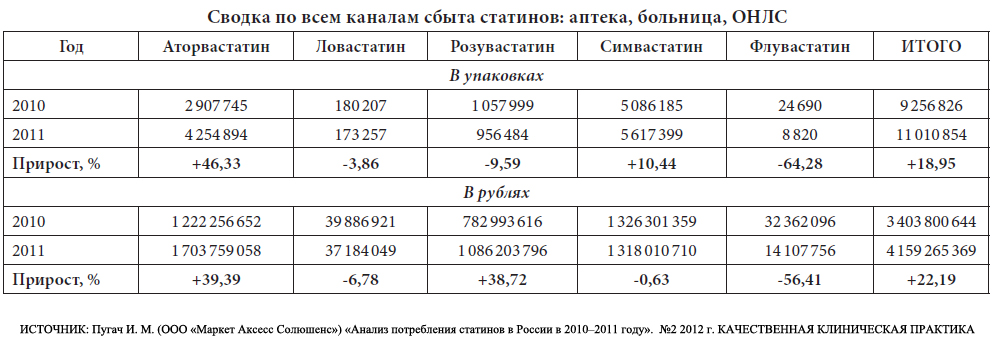
В подтверждение неуклонного роста "популярности" статиновых препаратов, обратимся к данным статистики… Ниже представлено несколько графиков (первые два — по США, третий по России)
Лечение статинами в последние годы при ишемической болезни сердца, атероматозе интимы коронарных артерий стало настолько распространенным [7], что даже предлагается назначать статины чуть ли не всем пациентам и даже в целях профилактики [8].
Так, например, в марте 2010 года, Администрация по контролю за продуктами и лекарствами США (FDA) одобрила [9, 10] новые показания для использования «Крестора», статина, производимого компанией Астра Зенека, второго по популярности статина в США (после пфайзеровского «Липитора»). В новом описании «Крестора» говорится, что он показан здоровым людям при соблюдении следующих трех условий: это мужчина старше 50 лет или женщина старше 60, это курильщик или гипертоник, это человек, в анализах которого наблюдаются признаки воспаления. Т.е. речь идет о применении статинов среди людей старше 50 лет, у которых пока нет каких либо проблем с холестерином и признаков сердечной патологии (в конце я более подробно расскажу об этом исследовании).
Более того, в число фармацевтические компании активно лоббируют применение статинов и среди детей [11, 12, 127]. По крайней мере в России, как минимум пока и вроде бы, лечение статинами детям противопоказано, исключением является гомозиготная форма семейной гиперхолестеринемии ЛПНП [13]. Также на уровне ВОЗ, сделан вывод, что статиновые препараты не соответствуют критериям, препаратов, применение которых может иметь важность для терапии среди детей [127].
Статины — вещества, специфически подавляющие активность 3-гидрокси-3-метилглутарил КоА редуктазы, фермента, необходимого для одного из первых этапов синтеза холестерина, — были открыты в 1976 году. В этот список входят ловастатин (мевакор), правастатин (правакол), симвастатин (зокор), флувастатин (лескол), аторвастатин (липитор). И он постоянно пополняется, несмотря на неоднозначные результаты применения статинов в клинической практике. [14]
На данный момент, статины, считаются главным медикаментозным препаратом, направленным на борьбу с повышенными уровнями холестерина в крови, который, как известно, на протяжении последних десятилетий был признан, главным врагом в развитии атеросклероза. Основной задачей применения статинов является снижение уровня «плохого» холестерина с целью уменьшения риска возникновения ишемической болезни сердца (ИБС) (первичная профилактика) или ее осложнений (вторичная профилактика).
Атеросклероз — процесс, лежащий в основе большинства заболеваний системы кровообращения (ишемия, инфаркт миокарда, тромбоз, инсульт мозга, гангрена нижних конечностей и др.) [15]. Согласно данным Всемирной Организации Здоровья, ключевым компонентом в развитии атеросклероза является холестерин, 18% всех случаев сердечнососудистых заболеваний сопровождается повышенным содержанием холестерина в крови, и в результате атеросклероза от ССЗ, ежегодно умирает порядка 4,4 миллиона людей.
Считается, что толчком [14] к изучению атеросклероза и, соответственно, холестерина послужили наблюдения врачей, сделанные во время войны между США и Кореей в 1950-е годы. У половины погибших американских солдат в возрасте 20–21 года при патологоанатомическом исследовании был обнаружен атеросклероз артерий сердца, причем у некоторых из них просвет сосудов был сужен более чем на 50%. После опубликования этих материалов в США начался «холестериновый бум». В 1988 году была создана и щедро финансировалась общенациональная программа США по борьбе с атеросклерозом. Программа включала в себя исследования по биохимии холестерина и по созданию «рациональной американской диеты» с исключением из пищи жиров, углеводов, соли и холестерина. Рекомендации время от времени модифицируются по мере накопления научных данных [16]. Правда в конце 2014 года произошло достаточно знаковое событие (по крайней мере, для Соединенных Штатов Америки), а именно, в новой версии «Диетических рекомендаций для американцев» (Dietary Guidelines for Americans)
холестерин больше не относится к списку опасных для здоровья нутриентов, хотя все равно, авторы доклада считают, что американцы употребляют слишком много насыщенного жира, потребление насыщенного жира все же предлагается ограничивать до 10% от всех потребляемых калорий.
Хотя, по сути, в основу «холестериновой» теории (согласно которой причиной образования атеросклеротических бляшек является проникновение холестерина в стенку сосуда), легли опыты, проведенные еще ранее, в начале ХХ века, группой русских ученых во главе с физиологом Н.А. Аничковым. Где ученые проводили эксперименты на кроликах [травоядные животные, для которых в основном не характерно, регулярное употребление животной пищи и холестерина], скармливая им холестерин [17]. После вскрытия, было обнаружено, что непосредственной причиной смерти, явилась закупорка кровеносных сосудов сердца сгустками жира, холестерина и солей кальция, напоминающие атеросклеротические повреждения сосудов человека (атероматозные бляшки). Стоит иметь ввиду, что другие животные – такие как крысы, собаки, бабуины не выдают такую же реакцию на высокохолестериновую диету, что и кролики, они усваивают холестерин совершенно иначе [67,68,69].
Под влиянием обменно-пищевой теории, или «липидно-инфильтрационной» теории [главенствующая теория атеросклероза; помимо этого еще существует, набирающая популярность [18] «воспалительная» или гомоцистеиновая теория, возникшая еще в 1969 году [14] см.сноску*], отводившей главную роль в развитии атеросклероза холестерину, поступающему в организм с пищей, было разработано множество диетических продуктов без холестерина и лекарств, снижающих его содержание в организме. Антихолестериновая теория породила, такие всем известные громкие лозунги, как «холестерин — убийца артерий», «холестерин — ужас века», «холестерин — общественная опасность номер один» и пр., а также рождение целой индустрии БАДов и так называемых «диетических» продуктов питания, не содержащих холестерина (вплоть до абсурдных, заявлений производителей продуктов питания, об отсутствии холестерина там, где он в принципе не может содержаться (растительное масло, овощи, фрукты и пр.). Ну и конечно главных и обязательных врачебных рекомендаций по профилактике и лечению атеросклероза — исключением из диеты любых богатых холестерином продуктов и заменой животных жиров на растительные.
С самого начала антихолестеринового бума, кол-во несогласных с этой теорией в мире науки, было достаточно велико. Годы исследований, позволили получить достаточно внушительный объем данных ставящих под сомнение роль холестерина в патогенезе атеросклероза. И несмотря на то, что роль холестерина как основного виновника атеросклероза уже перестала быть однозначной [19], все же «липидно-инфильтрационная» теория, все еще остается самой живучей и агрессивно активной.
Правда, все же теперь, ученые выделяют четыре определяющих механизма характерных для возникновении и формировании атеросклероза:
a) наследственный фактор,
b) нарушение липидного обмена,
c) состояние сосудистой стенки,
d) нарушение рецепторного аппарата клеток.
В каждом из них обнаружено не одно патологическое звено, формирующее в конечном итоге тот комплекс патогенетических факторов, которые определяют возникновение атеросклеротических изменений в стенке сосуда [20]. Многочисленными эпидемиологическими исследованиями было показано, что атеросклероз — это полиэтиологическое заболевание. Приписывание холестерину всех напастей в последние годы стало вызывать у специалистов, все больше и больше сомнений [14].
——————————
* СНОСКА: «Воспалительная» или гомоцистеиновая теория.
Согласно этой теории, атеросклероз — это вызываемый неспецифическим иммунитетом вялотекущий воспалительный процесс в стенках сосудов, который возникает в результате повреждения стенки сосуда (механическое, химическое или иммунологическое), что в свою очередь вызывает эндотелиальную дисфункцию. Нарушение функции эндотелия могут вызвать многие факторы: гемодинамические (артериальная гипертония), избыточный уровень гормонов (гиперинсулинемия), инфекции, токсичные соединения и др.; прямое воздействие со стороны модифицированных липопротеинов (гликозилированные ЛП (этому виду химической модификации подвержены все классы ЛП, но наиболее значительно — ЛПНП и ЛПВП), перекисно-модифицированные (окисленные) Х-ЛПНП (Холестерин ЛипоПротеидов Низкой Плотности), аутоиммунные комплексы ЛП-антитело, продукты ограниченного протеолиза ЛП, десиалированные Х-ЛПНП, комплексы Х-ЛПНП с гли-козаминогликанами, агрегированные ЛП); неэффективная утилизация ремнантных хиломикронов (остаточные хиломикроны, образующиеся после выхода из них триглицеридной «начинки», в результате естественных метаболических причин) [73].
Как известно самые мелкие липопротеиды, такие как ЛПВП, легко проникают в стенку сосуда, и так же легко ее покидают, не вызывая образования атеросклеротической бляшки. ЛПНП, ЛППП и ЛПОНП при модификации, легко задерживаются в сосудистой стенке. Модифицированные Х-ЛПНП, начинают восприниматься иммунной системой как «чужые» о-Х-ЛПНП с проявлением соответствующей защитной реакцией (воспалительный процесс): в присутствии цитокинов, высвобождаемых из моноцитов, внутренний слой кровеносных сосудов (эндотелий), выделяет адгезивные молекулы (липкие мелкие частицы), которые выполняют роль молекулярного клея для тех самых моноцитов; моноциты же в свою очередь далее превращаются в макрофаги; и вот эти самые макрофаги, уничтожают образовавшиеся о-Х-ЛПНП, сами же превращаясь в «пенистые» клетки, перегруженные окисленными фосфолипидами и холестерином [74]. «Бляшка» по сути это большое, давно образованное скопление «пенистых» клеток, и чем дольше длится воспаление, тем больше образуется «пенистых» клеток, что в свою очередь опять ведет к появлению большего числа макрофагов и липких липидных ядер. Некоторые «пенистые» клетки умирают, выпуская в кровь накопленные в себе окисленные фосфолипиды и холестерин, которые в свою очередь трансформируются в липидное ядро атеросклеротической бляшки (кстати, при попадании липидных ядер в кровь, чтобы купировать распространение этой субстанции, организм формирует тромб (сгусток крови)).
Это скажем так часть общего процесса. Там есть и прочие факторы и процессы, подробнее о чем можно прочесть в статье Анны Шаланда под названием "Холестериновая страшилка, которая правит миром". Там же подробно описано, что есть на самом деле холестерин, и почему его демонизация не имела и не имеет под собой сколь либо обоснованных оснований.
И кстати, коэнзим CoQ10, о котором еще пойдет речь далее в статье, синтез которого нарушают статиновые препараты, является мощным антиоксидантом, препятствующим окислительному повреждению Х-ЛПНП, и помогающему предотвратить описанные выше метаморфозы Х-ЛПНП в о-Х-ЛПНП.
И еще, эндотелиальная дисфункция у мужчин почти всегда сопряжена с эректильной дисфункцией, и боле того есть данные свидетельствующие о том, проблемы с эректильной дисфункцией, являются предиктом возникновения проблем с сердцем в течение ближайших 3-5 лет [70,71,72])
——————————
"Пара слов" о холестерине, для полноты общей картины [1, 2, 14].
1. Холестерин — это фабрика гормонов: холестерин, по сути, исходная молекула целого семейства гормонов, известных как стероидные гормоны, а также витамина D. Без него невозможно функционирование многих жизненно важных систем организма. В организме содержится до 350 гр. этого вещества. Только одну треть (примерно 0,3–0,5 гр. в день) необходимого холестерина мы получаем с пищей, а две трети (0,7–1 гр) синтезируем сами: 80% в печени, 10% в стенке тонкого кишечника и 5% в коже. Синтезом собственного холестерина организм компенсирует избыток или недостаток в рационе.
2. Организм использует холестерин для синтеза желчных кислот: желчные кислоты совершенно необходимы для усвоения жиров. Эти кислоты синтезируются из холестерина и затем секретируются в желчь. Желчные кислоты настолько важны для организма, что организм сам удерживает большую их часть. Он следит за тем, чтобы они не попали в экскременты, вызывая их обратное всасывание из нижнего отдела кишечника, помещая их в нечто вроде контейнера для «метаболической переработки» и направляя обратно в печень.
В печени из холестерина синтезируются желчные кислоты, необходимые для эмульгирования и всасывания жиров в тонком кишечнике. На эти цели уходит 60–80% холестерина. Материнское молоко богато холестерином. Грудные и растущие дети особенно нуждаются в богатых жирами и холестерином продуктах для полноценного развития мозга и нервной системы.
3. Холестерин — важнейшая составляющая всех клеточных мембран в организме: он особенно важен для мембран головного мозга (несмотря на то что вес самого мозга составляет лишь 2% от общей массы тела, в нем находится 25% всего холестерина организма), нервной системы, спинного мозга и периферических нервов. Он содержится в миелиновой оболочке, похожей на изолирующий материал или «покрытие» для нервных волокон, которая способствует передаче нервных импульсов; холестерин является неотъемлемой частью липидных плотов и в значительной степени способствует межклеточной коммуникации (в этом кроются причины такого множества трудностей, связанных с познавательным процессом, которые появляются при агрессивном снижении холестерина). Холестерин — важнейший элемент клеточных мембран мозга, и он играет ключевую роль в передаче нейротрансмиттеров. Холестерин также играет важную роль в обеспечении устойчивости клеток к перепаду температур.
4. Холестерин необходим иммунной системе: холестерин тесно связан с иммунной системой. Исследования показывают, что ЛПНП (так называемый «плохой» холестерин) в организме человека могут деактивировать более 90% самых плохих и наиболее токсичных бактерий, [21, 24] низкий уровень холестерина является показателем повышенного риска смерти от болезней дыхательных путей или желудочно-кишечного тракта — то есть от заболеваний, которые зачастую имеют инфекционное происхождение [22], люди с уровнем холестерина 4,14 ммоль/л и ниже имеют в четыре раза выше вероятность смерти от СПИДа, чем те, чей холестерин превышает 6,22 ммоль/л! (16 летнее экспериментальное исследование множественных факторов риска (MRFIT)) [23].
СТАТИНЫ: в чем виноваты статины и почему необходимо столь пристальное внимание к негативным эффектам которые может вызывать их прием?
Существует точка зрения, поддерживаемая достаточно большим кол-вом ученых, о том что статины значительно менее эффективны, чем принято об этом считать. И как не странно положительное воздействие, которое они могут оказать, имеет очень мало общего исключительно со снижением уровня холестерина (нет, холестерин то они снижают, но такое снижение, вряд ли можно назвать положительным эффектом, на фоне того комплексного влияния, которое оказывают статины, на организм в целом), у них имеется бессчетное количество неприятных, а в некоторых случаях острых — и даже смертельных — побочных эффектов, таких как мышечные боли, слабость, усталость, проблемы с памятью и познанием, очень серьезные проблемы с сексуальной активностью.
Все положительные результаты, насколько бы они ни были слабыми в реальности и переоцененными в рекламных материалах, практически всегда связаны именно с двумя эффектами, которые дают статины: первое, они снижают уровень С-реактивного белка (белка, содержащегося в крови, который служит идеальным индикатором воспаления), и, второе, они уменьшают вязкость крови, облегчая ее течение. По сути, если бы именно эти эффекты проявлялись при применении статинов, без подавления производства холестерина в организме, то положительная роль статинов, была бы значительно выше и продуктивнее.
Итак, сводное резюме о действии статинов может быть таким, статиновые препараты останавливают производство холестерина в организме, и сам по себе этот процесс не так уж и безобиден как это может показаться на первый взгляд. Достаточно красочная аналогия происходящих процессов, сродни попытке остановить рост верхней ветки дерева за счет иссушения его корней, а «побочным эффектом» такого голодания дерева будет его полное уничтожение, хотя основной комизм всей этой ситуации заключается в том, что изначально даже не было необходимости отрезать саму ветку.
Сам по себе, холестерин синтезируется в печени так называемым мевалонатным путем ("холестериновый коридор"), также известным как путь ГМГ-КоА-редуктазы. Фермент ГМГ-КоА-редуктазы несет непосредственную ответственность за инициацию производства холестерина, и именно этому ферменту и пытаются помешать статиновые препараты, технически известные как ингибиторы, то есть замедлители ГМГ-КоА-редуктазы.
Проблема заключается в том, что фермент ГМГ-КоА-редуктазы находится в основании мевалонатного пути, так же как ствол дерева является основанием, из которого растут все ветви. Если говорить о мевалонатном пути, из него «произрастает» множество других «ветвей», кроме холестериновой «ветки». Блокирование мевалонатного пути статинами, блокируется еще около 200 биохимических шагов к синтезу холестерина, а это означает, что, чтобы добраться до холестерина, статины прерывают многие другие жизненно важные функции обмена, использующие этот же путь. Мевалонатным путем производится не только холестерин, кроме того, этот путь отвечает за производство коэнзима Q10 — одного из наиболее важных питательных веществ для сердца. Прерывание мевалонатного пути у корня, также блокирует или снижает производство ядерного фактора каппа-В (NF- кВ), и нарушает работу путей, регулирующих производство таупротеина, долихолов и селенопротеина [2].
Безусловно [14], статины дают какой-то краткосрочный эффект, особенно у людей, страдающих генетически детерминированной гиперхолестеринемией, но в предупреждении и устранении атеросклероза их роль весьма сомнительна. И здесь необходимо отметить, что эти препараты вводились в широкую практику и прописывались миллионам пациентов в возрасте 50–60 лет, поскольку именно в этой возрастной категории самый высокий риск ССЗ [26]. Впоследствии, спустя десятилетия, длительный прием статинов обернулся для этих людей ослаблением памяти, повышенным риском болезни Паркинсона и болезни Альцгеймера [25, 27]. В результате чего, был сделан вывод, что статины действительно снижают риск ССЗ у людей среднего возраста, тогда как у людей в возрасте 75–85 лет способствуют повышению частоты их смертности [ниже будет более подробная информация о достаточно крупных многолетних контролируемых исследованиях].
О ПОБОЧНЫХ ЭФФЕКТАХ СТАТИНОВ
Итак, какие же основные побочные эффекты наблюдаются при применения статиновых препаратов, через замедление работы фермента ГМГ-КоА-редуктазы?
Liu J, Li A, Seneff S. Automatic Drug Side Effect Discovery from Online Patient-Submitted Reviews: Focus on Statin Drugs. IMMM 2011, The First International Conference on Advances in Information Mining and Management; October 23, 2011 to October 29, 2011; Barcelona, Spain. 2011 [51]
— снижение числа половых гормонов (мы помним, что все основные половые гормоны — тестостерон, прогестерон и эстроген — производятся при участии холестерина), в особенности тестостерона как у мужчин [39], так и у женщин [40]. Одно из исследований показало, что один из наиболее популярных статиновых препаратов повышал риск эректильной дисфункции минимум в два и максимум в семь раз [41]. Низкий уровень тестостерона связан с сокращением ожидаемой продолжительности жизни и повышением риска смерти от сердечно-сосудистых заболеваний [42]. Помимо прочего, имеются свидетельства об влиянии статинов на уменьшение выработки спермы у мужчин на 31% [63];
— снижение уровней холестерина, затрудняет проникновение в ткани и органы гормона окситоцина (т.н. "гомон любви"), через клеточные рецепторы (липидные плоты), посредством богатых холестерином мембран, т.е. без холестерина, эти самые "плоты" не могут функционировать должным образом (то же самое происходит с нейротрансмиттерами в мозгу, которым необходимы богатые холестерином мембраны для осуществления межклеточной коммуникации);
— статины блокируют деятельность серотониновых рецепторов в мозгу. Cеротониновые рецепторы — как и окситоциновые — закрепляются на богатых холестерином липидных плотах в клеточных мембранах, и снижение уровня холестерина, затрудняет попадание серотонина в клетки, статиновые препараты могут заблокировать деятельность серотониновых рецепторов [45]. По данным психиатров, величина 4,28 ммоль/л для общего холестерина является пограничной величиной, за которой следует зона депрессии и суицидальных попыток [43];
— статины вызывают проблемы с познавательными функциями и памятью — часто встречающиеся (и наверное, самые драматичные) побочные эффекты статиновых препаратов. Холестерин — важнейший элемент клеточных мембран мозга, и он играет ключевую роль в передаче нейротрансмиттеров, которые оказывают влияние на функции обработки информации и памяти. Существует прямая связь между холестерином и высвобождением нейротран-смиттеров, холестерин изменяет форму белков для стимуляции мыслительной деятельности и памяти [64]. Кстати этот факт, стоит иметь ввиду, тем врачам (в тех странах, где это не запрещено), которые рекомендуют давать статиновые препараты детям, чей мозг до двадцати пяти лет еще только развивается;
— низкие значения холестерина, часто характерны и для онкологической патологии [44];
— повышение уровней печеночных ферментов в крови (АСТ и АЛТ);
— миалгия – боль или мышечная слабость, не сопровождающаяся повышением уровня КФК (креатинкиназы);
— миопатия – наиболее серьезный побочный эффект терапии статинами, который может привести к рабдомиолизу. Известны факторы риска развития миопатии, к которым относят: одновременное назначение нескольких лекарственных средств одному пациенту, особенно полипрагмазия; приём статина в высокой дозе, пожилой возраст пациента, сахарный диабет как сопутствующее заболевание [28-31]. Дополнительными факторами риска являются те состояния, которые делают митохондрии более уязвимыми, более подверженными повреждению, например метаболический синдром, заболевания щитовидной железы и генетические мутации, связанные с митохондриальной дисфункцией [29]. Предполагается, что митохондриальная дисфункция может также лежать в основе многих других побочных эффектов статинов: когнитивные нарушения, невропатии, панкреатическая и печеночная дисфункция, половая дисфункция [29]. Вероятность развития и выраженность миопатии увеличиваются при сочетании терапии статинами и физических нагрузок [32-34,50]. Предполагается, что 25% пациентов с высокой физической активностью, принимающих статины, испытывают мышечную слабость, боли в мышцах и судороги [33]. Наряду с предположением, что статин-ассоциированная миопатия имеет невоспалительную природу, существует гипотеза об аутоиммунном характере повреждения миоцитов, т.е. статины инициируют аутоиммунный процесс [36,37]. Также возможные механизмы миотоксичности включают внутриклеточное истощение необходимых метаболитов и дестабилизацию клеточных мембран [35]. Весьма популярно на сегодняшний день представление о том, что статины могут оказывать неблагоприятное воздействие на метаболизм мышц, в том числе нарушать процесс окисления жирных кислот, уменьшать содержание кофермента Q10 (CoQ10) и усиливать деградацию белка в миоцитах путём изменения активности атрогина-1 и убиквитина [32,36];
— CoQ10. Истощение запасов CoQ10 — один из важных эффектов, оказываемых статинами на организм, и именно он в основном отвечает за множество распространенных побочных эффектов, в том числе мышечную боль, слабость и потерю энергии. Статины блокируют синтез фарнезила пирофосфата, промежуточного продукта в синтезе убихинона или CoQ10 (это происходит на одной из ветвей дерева мевалонатного пути). На этом, а также на роли CoQ10 в производстве энергии в митохондриях основана гипотеза, что статин-индуцированный дефицит CoQ10 имеет значение в патогенезе статиновой миопатии [57,58]. CoQ10 это соединение витаминного типа, содержащееся практически во всех клетках человеческого организма. Это мощный антиоксидант, который борется с повреждениями, полученными в результате окисления, возникающего по вине свободных радикалов, защищает клеточные мембраны, белки и ДНК, а также способствует увеличению производства организмом АТФ в клетке (выступая посредником между АТФ и кислородом). Предполагается, что статины вызывают митохондриальную дисфункцию, нестабильность мембран, нарушают экспрессию генов, отвечающих за апоптоз (происходит индукция апоптоза миоцитов) и деградацию белка [28, 30, 32, 33, 38]. Наиболее широко распространена гипотеза о том, что основной причиной развития миопатии является снижение внутримышечного содержания CoQ10 [30]. Кстати, от такой работы статинов наиболее страдают мышечные волокна типа IIb [126]. И еще, в сердце — концентрация CoQ10 максимальна, и существенное сокращение числа CoQ10, вызываемое статиновыми препаратами, наносит вред не скелетным мышцам, но и сердцу, т.е. органу, который эти препараты по идее должны защищать;
— рабдомиолиз – мышечные симптомы, характеризующиеся значительным повышением уровня КФК (обычно более чем в 10 раз), возрастанием уровня креатинина крови. Обычно рабдомиолиз сопровождается появлением мочи коричневого цвета, миоглобинурией. Последняя вызывает острую почечную недостаточность и в значительных случаях влечет за собой смерть больного;
— cуществуют также тревожные сигналы, указывающие на то, что статиновые препараты могут быть связаны с повышением риска возникновения рака и диабета [61,62], хотя доказательства этого далеко не неоспоримы. Исследователи из Медицинского департамента Медицинского центра Тафтса и медицинского факультета Университета Тафтса изучили двадцать три испытания статинов в поисках взаимосвязи между уровнем холестерина и раком. Они заключили, что «риск возникновения рака тесно связан со снижением уровня ЛПНП-холестерина», добавив при этом, что «преимущества для сердечно-сосудистой системы, которые она получает от снижения уровня ЛПНП-холестерина, частично нивелируются повышением риска возникновения рака» [59]. Кроме того, метаанализ пяти статиновых исследований показал, что с применением лечения с использованием статинов в больших дозах связан повышенный риск диабета [60]. То же открытие было сделано и в ходе известного испытания JUPITER, о котором я расскажу подробнее далее;
— из достаточно редких, но встречающихся, паралич Белла [65] (неврит лицевого нерва; идиопатическая, самая распространённая форма паралича лицевого нерва), опоясывающий герпес [66], а также транзиторная глобальная амнезия (ТГА). ТГА — это медицинский термин, описывающий редкий феномен, который может длиться от пятнадцати минут до двенадцати часов. Люди, испытывающие ТГА, внезапно теряют возможность фиксировать в памяти происходящие события и зачастую не могут узнать привычное окружение. Во многих случаях они даже не могут опознать членов собственной семьи, приходят в замешательство и плохо понимают, что происходит. Люди, испытывающие ТГА, буквально возвращаются во времени — на часы, дни, недели или даже годы — назад и не помнят ничего, что происходило после того момента, к которому они вернулись.
К факторам повышенного риска развития побочных эффектов статинов, в числе прочего, относятся [28]:
• пожилой возраст;
• дефицит массы тела;
• женский пол;
• почечная и/или печеночная недостаточность;
• полиорганная патология;
• гипотиреоз;
• периоперационный период;